
- 997556699
- [email protected]
medical devices
21
Oct
Oct

Perspectiva sobre las regulaciones de dispositivos médicos y dispositivos de diagnóstico in vitro en Perú
by Pharma Consulting | dispositivos médicos, registro sanitario | 0 Comment
En Perú, la Dirección General de Medicamentos, Insumos y Medicamentos (DIGEMID) supervisa el mercado de dispositivos médicos y dispositivos de diagnóstico in vitro. Esta agencia registra dispositivos, emite licencias de operación, inspecciona las instalaciones de fabricación y los almacenes, monitorea las pruebas de productos y redacta políticas y leyes con respecto a los dispositivos médicos
13
Jul
Jul
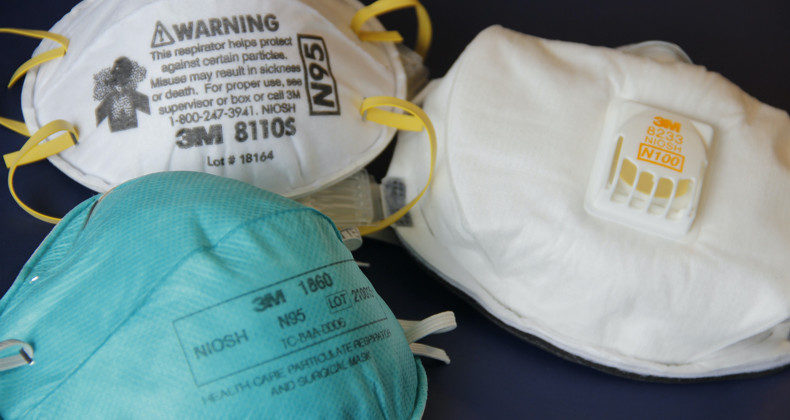
Respiradores de uso médico N95, FFP2 y KN95 deben contar con registro sanitario de DIGEMID
by Pharma Consulting | COVID-19, dispositivos médicos | 0 Comment
La Dirección de Medicamentos, Insumos y Drogas - DIGEMID, ha establecido el registro obligatorio de respiradores para uso médico a partir del 1 de enero de 2021. Este mandato afecta a instituciones y establecimientos farmacéuticos que importan, almacenan, fabrican o comercializan respiradores N95, KN95, FFP2 o FFP3 para uso médico y similares, ya que se
19
Oct
Oct

DIGEMID redujo el periodo de evaluación para el registro de dispositivos médicos en Perú
La Autoridad Nacional de Medicamentos, DIGEMID, ha reducido el plazo máximo de evaluación para la inscripción y reinscripción de dispositivos médicos en el registro sanitario. Dispositivos médicos (MD) Clase I, bajo riesgo: hasta treinta (30) días calendario. Dispositivos médicos (MD) Clase II, riesgo moderado: hasta sesenta (60) días calendario. Dispositivos médicos (MD) Clase III, alto
20
Sep
Sep

DIGEMID permite la venta directa de dispositivos médicos a pacientes, IPRESS, profesionales y distribuidores
by Pharma Consulting | biomedical equipment, dispositivos médicos, e-commerce, medical devices | 0 Comment
DIGEMID, mediante la R.D. No. 033-2017-DIGEMID-DG-MINSA, publicado a principios de este año, emitió una lista de dispositivos médicos que pueden comercializarse directamente a los usuarios finales. Este documento no lista todos los dispositivos médicos, pero establece un criterio basado en la clasificación de riesgo de los dispositivos médicos. Dispositivos médicos de clase I, II, III
20
Aug
Aug
DIGEMID aprueba listado de dispositivos médicos que se pueden comercializar directamente al usuario final
La Dirección de Medicamentos, Insumos y Drogas - DIGEMID, emitió una lista de dispositivos médicos que pueden comercializarse directamente a los usuarios finales. Para adquirir un producto en particular, los usuarios deben presentar una receta médica, si es necesario. Equipo Biomédico Equipos biomédicos de clase I (riesgo bajo), clase II (riesgo moderado), clase III (alto