Póngase en contacto con nosotros
para brindarle más información sobre nuestros servicios.

Póngase en contacto con nosotros
para brindarle más información sobre nuestros servicios.
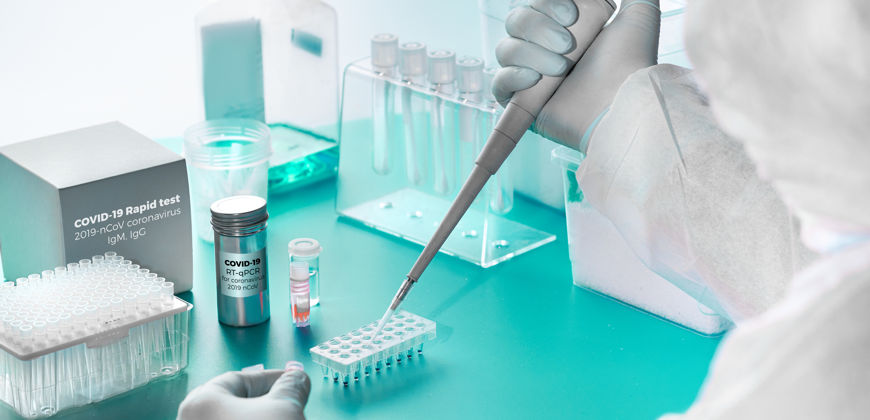
El registro sanitario es la autorización emitida por DIGEMID a solicitud de una droguería o laboratorio y que faculta a su titular la fabricación, importación, almacenamiento, comercialización, promoción y expendio de un dispositivo médico de diagnóstico in vitro (IVD) específico.
Los dispositivos médicos de diagnóstico in vitro (IVD) importados deben estar registrados en DIGEMID antes de ser comercializados en nuestro país. Esta categoría incluye reactivos utilizados para el diagnóstico clínico en hematología, patología, inmunología y medicina nuclear.
Las inscripciones en el registro sanitario deben renovarse cada 5 años.
Esbozaremos la estrategia regulatoria óptima para sus productos, de acuerdo con su clasificación de riesgo.
Evaluación de la documentación técnica y científica emitida por el fabricante.
Preparación de un expediente de registro completo y envío de la solicitud de registro a DIGEMID a través de VUCE.
Seguimiento de solicitudes de registro. Respuesta a las consultas y observaciones de los evaluadores de DIGEMID.
Productos IVD, pruebas rápidas, autotests, analizadores de bioquímica, reactivos y insumos.
Dispositivos médicos Clase I, II, III y IV. Equipos biomédicos, odontológicos y sistemas electromédicos.
Pañitos húmedos, pañales desechables, protectores de lactancia y pañitos desmaquillantes.
Productos biológicos, sustitutos del azúcar y suplementos dietéticos.